Бронхиальная астма
У термина «болезнь» есть много синонимов, в том числе заболевание, недуг, расстройство, патология и другие. Все они описывают любое внешнее или внутреннее изменение, которое мешает нормальному функционированию организма человека. Существует множество обязательных факторов, которые необходимы для того, чтобы человек оставался здоровым. Среди них чистые воздух и вода, правильный рацион питания, соблюдение правил личной гигиены, адекватные физические нагрузки и др.
Прежде всего из рациона следует исключить продукты, вызывающие аллергическую реакцию. При аспириновой астме исключают продукты, содержащие салицилаты и тартразин. При всех формах бронхиальной астмы ограничивают употребление продуктов, содержащих гистамин (вино, консервы, копчености, шпинат, помидоры, квашеная капуста), а также способствующие высвобождению гистамина (яйца, раки, клубника, шоколад, бананы, орехи, арахис, алкоголь, бульоны, приправы, кофе, чай). Целесообразно употребление продуктов, содержащих пищевые волокна и пектины (цельные злаки, крупы, овощи, ягоды и фрукты, сухофрукты, дикорастущие съедобные травы). Наиболее эффективный способ терапии бронхиальной астмы изложен в Рекомендациях Европейского респираторного общества и Национального института здоровья (США) по лечению астмы. Они заключаются в постоянном и поэтапном (ступенчатом) лечении больного.
Ступень № 1.
Интермиттирующая бронхиальная астма, легкое течение заболевания (эпизодическая астма)
Клиническая картина до начала лечения. Симптомы астмы (приступы удушья) возникают эпизодически, быстро исчезают и бывают реже 1 раза в неделю. Кратковременные обострения — от нескольких часов до нескольких дней. Симптомы астмы возникают в ночное время и бывают реже 2 раз в месяц.
Отсутствие симптомов и нормальная функция легких в периоды между обострениями. Пиковый максимальный поток выдоха (ПМПВ), определенный пикфлуориметром, или объем форсированного выдоха за 1 с (ОФВ,) в норме или близки к норме в период между обострениями: около 80 % и более от должных величин, отклонение — менее 20 %.
При описанной клинической картине для купирования редких приступов удушья и прежде всего для их предупреждения показано следующее лечение:
- Избегать контакта с пусковыми (аллергическими и др.) факторами.
- По «требованию больного» при наличии симптомов не более 1 раза в неделю ингалировать р2-адреномиметики короткого действия: сальбутамол (син.: вентолин, саламол) в аэрозольных баллонах по 10 мл, содержащих 200 доз: 1 дозу (ОД мг), реже 2 дозы (соответственно 1—2 вдоха препарата); фенотерол (син. беротек) в аэрозольных баллонах по 15 мл, содержащих 300 доз: по одному вдоху (0,2 мг препарата); тербуталин (син.: бриканил, арубендол) в аэрозольных баллонах: один вдох.
- Перед физической нагрузкой или перед предстоящим воздействием аллергена ингалировать Р2-адреномиметики короткого действия (см. п. 2) или кромолин-натрий (син.: кромогликат натрия, интал, кромолин, ломузол): ингалировать 1 капсулу порошка (0,02 г) карманным турбоингалятором «Спингалер».
При более выраженной клинической картине и в случае необходимости применения симпатомиметиков более 2—3 раз в неделю рекомендуют переход на вторую ступень фармакотерапии бронхиальной астмы.
Ступень № 2.
Персистирующая бронхиальная астма, легкое течение заболевания
Клиническая картина до начала лечения. Частота обострений, нарушающих активность и сон больного, 1—2 раза в неделю. Симптомы астмы возникают 1 раз в неделю или чаще, но реже 1 раза в день, в ночное время 1—2 раза в месяц.
Симптомы постоянные, не резко выраженные, но персистирующие. Хронические симптомы, требующие почти ежедневного введения Р2-агонистов короткого действия. ПМПВ или ОФВ, в пределах более 80 % от должных величин, отклонение — 20—30 %.
Лечение. 1. Аэрозольное противовоспалительное средство ежедневно: сначала ингаляционные кортикостероиды (беклометазона дипропионат, бекотид, бекломет, беклат — аэрозоль на 200 ингаляций: по 200—500 мкг в сутки или недокромила натрий (син. тайлед) — аэрозоль в баллонах: по 1—2 дозе (в каждой дозе 2 мг) либо кромолин-натрий (син.: кромогликат натрия, интал, кромолин, ломузол): ингалировать 1 капсулу порошка (0,02 г) карманным турбоингалятором «Спингалер». Подобное недокромилу натрия действие имеет кетотифен (син.: задитен, астафен) в капсулах и таблетках: по 0,001 г внутрь во время еды 2 раза в сутки. У детей начинают лечение с назначения пробных доз кромолин-натрия.
2. При отсутствии эффекта от проводимой терапии или незначительном эффекте дозу ингаляционных кортикостероидов повышают от 250—500 мкг до 750 мкг в сутки. Если симптомы астмы в ночное время остаются, то переходят на ступень № 3 с добавлением:
1) бронходилататоров длительного действия. Вольмакс в таблетках по 0,008 г: по 8 мг внутрь 2 раза в сутки, формотерол по 12—24 мг для ингаляции 2 раза в сутки или по 20—40 мг внутрь 1—2 раза в сутки, сальметерол (серевент) в порошке по 50 мкг для ингаляции 2 раза в сутки, а также препараты теофиллина пролонгированного действия:
а) препараты теофиллина 1-го поколения для приема внутрь: тео-дур, теотард в таблетках и капсулах: по 300 мг 2 раза в сутки; дурофиллин в капсулах: по 250 мг 2 раза в сутки; вентакс в капсулах, самофиллин по 200 мг 2 раза в сутки; теопэк, ретафил в таблетках: по 300 мг 2 раза в сутки;
б) препараты теофиллина 2-го поколения для приема внутрь: филоконтин по 100—350 мг 1 раз в сутки; эуфилонг в капсулах по 0,25 г: по 250—500 мг 1 раз в сутки; дилатран, унифил по 200—400 мг 1 раз в сутки; тео-24 по 1200—1500 мг 1 раз в сутки.
2) ингаляционные Р2-адреномиметики короткого действия, которые вводят по требованию больного, но не чаще 3—4 раз в сутки: сальбутамол, фенотерол, тербуталин (см. п. 2 ступени № 1).
Ступень № 3.
Персистирующая бронхиальная астма средней тяжести
Клиническая картина до начала лечения. Симптомы астмы наблюдаются почти ежедневно. Симптомы астмы в ночное время появляются чаще 1—2 раз в неделю. Обострения вызывают нарушение активности и сна. ПМПВ или ОФВ, в пределах 60—80 % от должных величин, отклонение — более 30 %.
Лечение. 1. Увеличить суточную дозу противовоспалительных средств: ингаляционные кортикостероиды — беклометазона дипропионат, бекотид, бекломет, беклат в аэрозоли на 200 ингаляций: по 200—800 мг, иногда до 1000 мкг в сутки (более 1000 мкг под наблюдением врача).
2. При наличии симптомов в ночное время назначают теофиллин пролонгированного действия (см. п. 1 ступени № 2):
а) препараты теофиллина 1-го поколения для приема внутрь: тео-дур, теотард в таблетках и капсулах: по 300 мг 2 раза в сутки; дурофиллин в капсулах по 0,25 г: по 250 мг 2 раза в сутки; вентакс в капсулах, самофиллин по 200 мг 2 раза в сутки; теопэк, ретафил в таблетках: по 300 мг 2 раза в сутки;
б) препараты теофиллина 2-го поколения для приема внутрь: филоконтин по 100—350 мг 1 раз в сутки; эуфилонг в капсулах по 0,25 г: по 250—500 мг 1 раз в сутки; унифил по 200—400 мг 1 раз в сутки.
3. При наличии ночных приступов назначают перорально Р2-агонисты длительного действия: вольмакс в таблетках по 0,008 г: по 8 мг 2 раза в сутки, формотерол по 12—24 мг для ингаляции 2 раза в сутки или по 20—40—80 м г внутрь 2 раза в сутки.
4. Возможно применение ингаляционных м-холиноблокирующих средств: ипратропия бромида (син.: атровент, итроп) в аэрозольных баллонах по 15 мл: по 2 вдоха (2 раза по 20 мкг) 3—4 раза в сутки; тровентола (трувент) в аэрозольных баллонах по 21 мл: по 1—2 вдоха 2 раза в сутки.
5. Ингаляционные Р2-адреномиметики короткого действия (сальбутамол в аэрозольных баллонах по 10 мл, фенотерол в аэрозольных баллонах по 10 мл, фенотерол в аэрозольных баллонах по 15 мл, тербуталин; см. п. 2 ступени № 1) вводят по требованию больного до 3—4 раз в сутки.
Ступень № 4.
Персистирующая бронхиальная астма, тяжелое течение
Клиническая картина до начала лечения. Частые обострения.
Постоянное наличие дневных симптомов. Частое возникновение симптомов астмы (приступов) в ночное время. Физическая активность ограничена. ПМПВ или ОФВ, менее 60 % от должных величин, отклонение составляет более 30 %.
Лечение. 1. Увеличить суточную дозу противовоспалительных средств: ингаляционные кортикостероиды — беклометазона дипропионат, бекотид, бекломет, беклат, будесонид, флютиказона пропионат, фликсотид в аэрозольных баллонах: по 800—1000 мг (от 1000 до 2000 мкг под наблюдением врача).
2. При наличии симптомов в ночное время назначают теофиллин пролонгированного действия (см. п. 1 ступени № 2):
а) препараты теофиллина 1-го поколения для приема внутрь: тео-дур, теотард по 300 мг 2 раза в сутки; дурофиллин в капсулах по 0,25 г: по 250 мг 2 раза в сутки; вентакс в капсулах, самофиллин по 200 мг 2 раза в сутки; теопэк, ретафил в таблетках: по 300 мг 2 раза в сутки;
б) препараты теофиллина 2-го поколения для приема внутрь: филоконтин по 100—350 мг 1 раз в сутки; эуфилонг в капсулах по 0,25 г: по 250—500 мг 1 раз в сутки; дилатран, унифил по 200—400 мг 1 раз в сутки; тео-24 по 1200—1500 мг 1 раз в сутки.
3. При наличии ночных приступов назначают:
а) пероральные р2-адреномиметики длительного действия (см. п. 3 ступени № 3): вольмакс в таблетках по 0,008 г: по 8 мг 2 раза в сутки, формотерол по 12—24 мг для ингаляции 2 раза в сутки или по 20—40—80 мг внутрь 2 раза в сутки или
б) ингаляционные Р2-адреномиметики длительного действия: формотерол по 12—24 мг для ингаляции 2 раза в сутки или по 20—40 мг внутрь 1—2 раза в сутки, сальметерол (серевент) в порошке: по 50 мкг для ингаляции 2 раза в сутки.
4. Ингаляционные Р2-адреномиметики короткого действия: сальбутамол в аэрозольных баллонах по 10 мл, фенотерол в аэрозольных баллонах по 15 мл, тербуталин в аэрозольных баллонах (см. п. 2 ступени № 1) вводят по требованию больного, но не чаще 3—4 раз в сутки. Повышение потребности в этих препаратах указывает на необходимость усиления противовоспалительной терапии.
5. Возможно применение ингаляционных холиноблокаторов (см. п. 4 ступени № 3): ипратропия бромид (син.: атровент, итроп) в аэрозольных баллонах по 15 мл: по 2 вдоха (2 раза по 20 мкг) 3—4 раза в сутки; тровентол (трувент) в аэрозольных баллонах по 21 мл: по 1—2 вдоха 3 раза в сутки.
6. Кортикостероиды внутрь через день или 1 раз в сутки в течение длительного времени:
а) короткого действия: кортизон в таблетках по 0,025— 0,05 г, преднизолон в таблетках по 0,001—0,005 г, метилпреднизолон (метипред, урбазон) в таблетках по 0,004 г;
б) средней продолжительности действия: триамцинолон в таблетках по 0,004 г;
в) длительного действия: дексаметазон в таблетках по 0,0005 г.
«Шаг вниз». Если на той или иной ступени получен хороший лечебный эффект и он сохраняется в течение нескольких месяцев, то возможен осторожный переход на более низкую ступень с тем, чтобы определить минимально необходимый объем терапии для поддержания достигнутого эффекта. Если контроль симптомов и функциональных нарушений системы дыхания невозможен, следует перейти на более высокую ступень лечения. Следует рассказать больному о симптомах, которые указывают на ухудшение состояния, а также о мерах, которые следует предпринять в таких случаях. Кроме изложенной схемы терапии бронхиальной астмы, в ряде случаев эффективны энтеро, гемо, иммуно, плазмосорбция, гемофильтрация, плазма, лимфоферез. УФО аутокрови, внутрисосудистое лазерное облучение крови, экстракорпоральная перфузия ксеноселезенки. Иногда назначают антигистаминные препараты (см. Аскаридоз легких), применяют иглорефлексо, баротерапию, санаторнокурортное лечение. Всем больным рекомендуют психотерапевтическое лечение, иногда в сочетании с транквилизаторами: хлозепид (син.: либриум, напотон, элениум) в таблетках по 0,005 г: по 0,005—0,01 г в сутки, мезапам (син. рудотель) в таблетках по 0,01 г: по 0,02—0,03 г в сутки, мепротан (син.: мепробамат, андаксин) в таблетках по 0,2 г: по 0,2—0,4 г внутрь 2—3 раза в сутки.
Обязательна санация ЛОР-органов и очагов хронической инфекции. При наличии вязкой и трудноотходимой мокроты рекомендуют отхаркивающие и муколитические средства (см. Бронхит острый). При атопической астме рекомендуют этимизол в таблетках по 0,1 г: по 100 мг 3 раза в сутки. Специфическую гипосенсибилизацию проводят гистаглобулином по 2 мл (до 3 мл) под кожу с интервалом 2—3 дня, на курс лечения 7—10 инъекций. Для предупреждения образования микротромбов показаны гепарин (во флаконах по 5 мл): по 5000— 10 000 ЕД 2—3 раза в сутки, дипиридамол (син. курантил) в таблетках по 0,025 г: по 0,025—0,05 г внутрь 3 раза в сутки. В межприступный период назначают электрофорез кальция и брома по Вермелю (анод располагают между лопатками) по 20—30 мин через день или магния и серы (анод располагают между лопатками) по 20—30 мин через день. Показана электропирексия УВЧ-полем по 1,5—3 ч 1 раз в 3 дня (на курс лечения 5—10 сеансов, перед началом сеанса выяснить переносимость больным высокой температуры тела), переднезадняя диатермия на область грудной клетки или индуктотермия по 20 мин через день. При выраженной сенсибилизации назначают диатермию на область селезенки по 10—20 мин через день. Показаны также ультразвук на боковые поверхности грудной клетки и паравертебральные области, электросон (5—10 импульсов за 1 с) по 30 мин ежедневно, общее УФО для стимуляции деятельности коркового вещества надпочечников или УФО области грудной клетки, а также аэроионизация дыхательных путей с необходимыми лекарственными растворами (щелочи, антисептики, травяные отвары).
При выраженных аутоиммунных процессах, несмотря на глюкокортикостероидную терапию, крайне редко прибегают к применению азатиоприна (син. имуран) в таблетках по 0,05 г, меркаптопурина в таблетках по 0,05 г: вначале по 50 мг в сутки, затем через 3 дня при отсутствии лейкопении и тромбоцитопении суточную дозу препарата увеличивают до 100 мг, а еще через 3 дня до 150 мг в сутки. Курс лечения 3—4 нед, если позволяет количество лейкоцитов и тромбоцитов в периферической крови, которое контролируют каждые 3 дня. Хирургическое лечение бронхиальной астмы себя не оправдало.
Источник
ДИАГНОСТИКА И СТУПЕНЧАТЫЙ ПОДХОД К КЛАССИФИКАЦИИ И ЛЕЧЕНИЮ БРОНХИАЛЬНОЙ АСТМЫ
*Импакт фактор за 2018 г. по данным РИНЦ
Читайте в новом номере
Несмотря на четкое определение бронхиальной астмы, достаточно яркие симптомы и возможности функциональных методов исследования диагностика заболевания вызывает трудности.
Despite the fact that bronchial asthma is well defined, its rather obvious symptoms and the capacities of functional techniques present some difficulties in diagnosing the disease. The paper outlines currently available approaches to making the diagnosis of bronchial asthma, its classification, and treatment by applying a stepwise approach.
Н. П. Княжеская, кафедра госпитальной терапии педиатрического факультета РГМУ, Москва
N.P. Knyazhevskaya, Department of Hospital Therapy, Russian State Medical University
Б ронхиальная астма — хроническое воспалительное заболевание дыхательных путей, в котором принимают участие многие клектки: тучные, зозинофилы, Т-лимфоциты. У предрасположенных лиц это воспаление приводит к повторяющимся эпизодам хрипов, одышки, тяжести в грудной клетке и кашлю, особенно ночью и/или ранним утром. Эти симптомы обычно сопровождаются распространенной, но вариабельной обструкцией бронхиального дерева, которая частично или полностью обратима спонтанно или под влиянием лечения [1].
Как показывают эпидемиологические исследования, несмотря на четкое определение заболевания, достаточно яркие симптомы и большие возможности функциональных методов исследования, бронхиальную астму плохо диагностируют, а следовательно, и плохо лечат [2]. Наиболее часто астму диагностируют как различные формы бронхита и как следствие этого неэффективно и неадекватно лечат курсами антибиотиков и противокашлевых препаратов [3 — 5]. Таким образом, распространенный тезис о том, что «все, что сопровождается свистящими хрипами, еще не является бронхиальной астмой», необходимо изменить на более соответствующий: «все, что сопровождается свистящими хрипами, следует считать астмой до тех пор, пока не будет доказано обратное» [1].
В постановке диагноза бронхиальной астмы существенное значение придается анамнезу и оценке симптомов заболевания. Наиболее распространенными симптомами являются эпизодические приступы удушья, одышки, появление свистящих хрипов, ощущение тяжести в грудной клетке, а также кашель. Однако сами по себе эти симптомы еще не являются диагнозом. Важный клинический маркер бронхиальной астмы — исчезновение симптомов спонтанно или после применения бронходилататоров и противовоспалительных препаратов. При оценке и сборе анамнеза значение придается следующим фактам: повторные обострения, чаще всего провоцируемые аллергенами, ирритантами, физической нагрузкой или вирусной инфекцией, а также сезонная вариабельность симптомов и наличие атопических заболеваний у родственников [1, 6, 7].
Поскольку симптомы астмы меняются в течение дня, нормальные данные можно получить при физикальном обследовании. Во время обострения астмы спазм гладкой мускулатуры, отек и гиперсекреция ведут к обструкции мелких бронхов, аускультативно врач чаще всего выслушивает сухие хрипы. Однако необходимо помнить, что у некоторых больных даже в период обострения при аускультации хрипы могут не выслушиваться, в то время как с помощью объективных исследований будет зарегистрирована значительная бронхообструкция, вероятно, за счет преобладающего вовлечения в процесс мелких дыхательных путей. Поэтому измерение функции внешнего дыхания (ФВД) обеспечивает объективную оценку бронхообструкции, а измерение ее колебаний — непрямую оценку гиперреактивности дыхательных путей. Существует широкий диапазон различных методов оценки степени бронхиальной обструкции, но наиболее широкое применение получили измерение объема форсированного выдоха за 1 с (ОФВ1) и связанное с ним измерение форсированной жизненной емкости легких (ФЖЕЛ), а также измерение форсированной (пиковой) скорости выдоха (ПСВ) [8].
Вероятно наиболее важное нововведение в диагностике и контроле бронхиальной астмы — это появление пикфлоуметра. Регулярный домашний мониторинг полезен, так как он помогает врачам и пациентам выявить ранние признаки ухудшения состояния и принять необходимые препараты.
Многие исследования продемонстрировали, что предъявляемые пациентами жалобы не соответствуют степени бронхиальной обструкции.
Неправильная оценка степени тяжести течения астмы самим больным и его врачом является основным фактором, обусловливающим недостаточно адекватное противовоспалительное лечение, и может привести к тяжелому обострению или даже к летальному исходу. Применение пикфлоуметрии позволяет достаточно точно диагностировать и классифицировать тяжесть течения бронхиальной астмы и соответственно назначать противовоспалительную поддерживающую терапию с учетом тяжести заболевания, т. е. осуществлять так называемый ступенчатый подход [9].
Наряду с оценкой симптомов, анамнеза физикальных данных и показателей ФВД для постановки диагноза имеет большое значение изучение аллергологического статуса. Наиболее часто используются скарификационные, внутрикожные и уколочные (прик-тест) тесты.
Однако в ряде случаев кожные тесты приводят к ложнонегативным или ложнопозитивным результатам. Поэтому часто проводится исследование специфических IgE-антител в сыворотке крови.
| Диагностика астмы строится на основании анализа симптомов и анамнеза, а также исследовании ФВД. Наиболее важными легочными функциональными тестами являются выявление ответа на ингаляции b 2 -агонистов, изменение вариабельности бронхиальной проходимости с помощью мониторирования ПСВ, провокации с помощью физической нагрузки у детей. Ценным дополнением к диагностике является определение аллергологического статуса. |
Как было уже сказано, бронхиальную астму довольно часто неправильно диагностируют и как следствие этого назначают неправильную терапию. Особенно трудно диагностировать астму у детей, пожилых людей, а также при воздействии профессиональных факторов риска, сезонности заболевания и при кашлевом варианте астмы.
Диагностика астмы у детей представляет чаще всего большие трудности в связи с тем, что эпизоды свистящих хрипов и кашель являются наиболее частыми симптомами детских болезней. Помощь в постановке диагноза оказывает выяснение семейного анамнеза, атопического фона. Повторные приступы ночного кашля у детей, в остальном практически здоровых, почти наверняка подтвержают диагноз бронхиальной астмы [10]. У некоторых детей симптомы астмы провоцирует физическая нагрузка [11].
Другой группой больных, в которой диагноз астмы (при позднем начале) врач или не ставит, или пропускает, являются люди пожилого возраста. У них трудно не только диагностировать астму, но и оценить тяжесть ее течения. Тщательный сбор анамнеза, обследование, направленное на исключение других заболеваний, сопровождающихся подобной симптоматикой (прежде всего ишемической болезни сердца с признаками левожелудочковой недостаточности), а также функциональные методы исследования, включающие также регистрацию электрокардиограмм и проведение рентгенологического исследования, обычно проясняют картину [12].
Диагностика профессиональной астмы также представляет определенную сложность. Известно, что многие химические соединения, присутствуя в окружающей среде, вызывают астму.
Они варьируют от высокоактивных низкомолекулярных соединений, таких как изоцианаты, до известных низкомолекулярных соединений, таких как изоцианаты, до известных иммуногенов, таких как соли платины, растительных комплексов и продуктов животного происхождения. Для постановки диагноза нужен четкий анамнез: отсутствие симптомов до начала работы, подтвержденная связь между развитием симптомов астмы на рабочем месте и их исчезновением после ухода с данного рабочего места. Точно подтвердить диагноз бронхиальной астмы можно при помощи исследования показателей ФВД: измерения ПСВ на работе и вне рабочего места, проведение специфических провокационных тестов. Следует учитывать, что даже при прекращении воздействия повреждающего агента сохраняется и продолжает ухудшаться течение бронхиальной астмы. Поэтому очень важны ранняя диагностика профессиональной астмы, прекращение контакта с повреждающим агентом, а также рациональная фармакотерапия.
Сезонная астма обычно связана с аллергическим ринитом. В период между сезонами симптомы бронхиальной астмы могут полностью отсутствовать. При постановке диагноза большое значение имеют анамнез и углубленное аллергообследование, а также измерение показателей ФВД и проведение ингаляционных тестов с b 2-агонистами в период обострения.
Кашлевой вариант астмы представляет значительную трудность в диагностике данного заболевания. Кашель практически является основным, а иногда и единственным симптомом. У таких больных кашель часто возникает в ночные часы и, как правило, не сопровождается свистящими хрипами. При исследовании показетелей ФВД в дневные часы часто регистрируются нормальные значения. Для правильной постановки диагноза большое значение имеет определение вариабельности показателей ФВД в сочетании с поисками эозинофилов в мокроте и диагностическими тестами для выявления гиперчувствительности [13].
Классификация бронхиальной астмы проводится на основании этиологии, тяжести течения и особенностей проявления бронхиальной обструкции. В прошлые годы из-за отсутствия понимания основополагающих процессов, происходящих при астме, основной упор делали на более очевидные проявления бронхиальной астмы, а именно на острое воспаление, бронхоспазм и ограничение воздушного потока [14]. Это привело к преимущественному использованию бронходилататоров для коррекции всех проявлений астмы. В настоящее время известно, что воспаление воздушных путей подразумевает как обострение, так и хроническое течение астмы. В связи с этим произошло изменение подходов к лечению болезни по направлению к длительному использованию противовоспалительных лекарств. Для подбора адекватной противовоспалительной терапии важно определить тяжесть течения бронхиальной астмы. Ни один тест не позволит точно классифицировать степень тяжести бронхиальной астмы. Однако комбинирование оценки симптомов и показателей ФВД дает характеристику болезни в зависимости от степени тяжести.
Установлено, что оценка течения бронхиальной астмы, основанная на клинических проявлениях болезни, связана с показателями степени воспаления дыхательных путей [15].
Как уровень обструкции, так и степень ее обратимости позволяют подразделить астму по степени тяжести на интермиттирующую, легкую персистирующую (хронического течения), средней тяжести (умеренную) и тяжелую [16]. При лечении астмы в настоящее время применяют ступенчатый подход, при котором интенсивность терапии увеличивается по мере увеличения степени тяжести астмы (рис. 1).
| Ступенчатый подход к терапии астмы рекомендуется в связи с большим разнообразием тяжести течения астмы у различных людей и у одного и того же пациента в разные временны’е периоды. Цель такого подхода — достижение контроля над заболеванием с применением наименьшего количества препаратов. Количество и частота приема лекарств увеличиваются (ступень вверх), если течение астмы ухудшается, и уменьшается (ступень вниз), если течение астмы хорошо контролируется. Ступенчатый подход также предполагает необходимость избегать или контролировать триггеры на каждой ступени. |
После определения тяжести течения астмы у больного (см. рис. 1) врач должен решить вопрос о том, стоит ли проводить вначале максимальное лечение для наиболее быстрого достижения контроля над астмой с последующим снижением препаратов (ступень вниз) или начать лечение с небольшого объема лекарств, а затем усиливать его (ступень вверх) при необходимости. В любом случае если удается контролировать симптомы астмы в течение 3 мес, то можно тщательно обдумать вопрос об уменьшении терапии (ступень вниз). Переход на более низкую ступень позволяет установить наименьший объем терапии, необходимый для контроля.
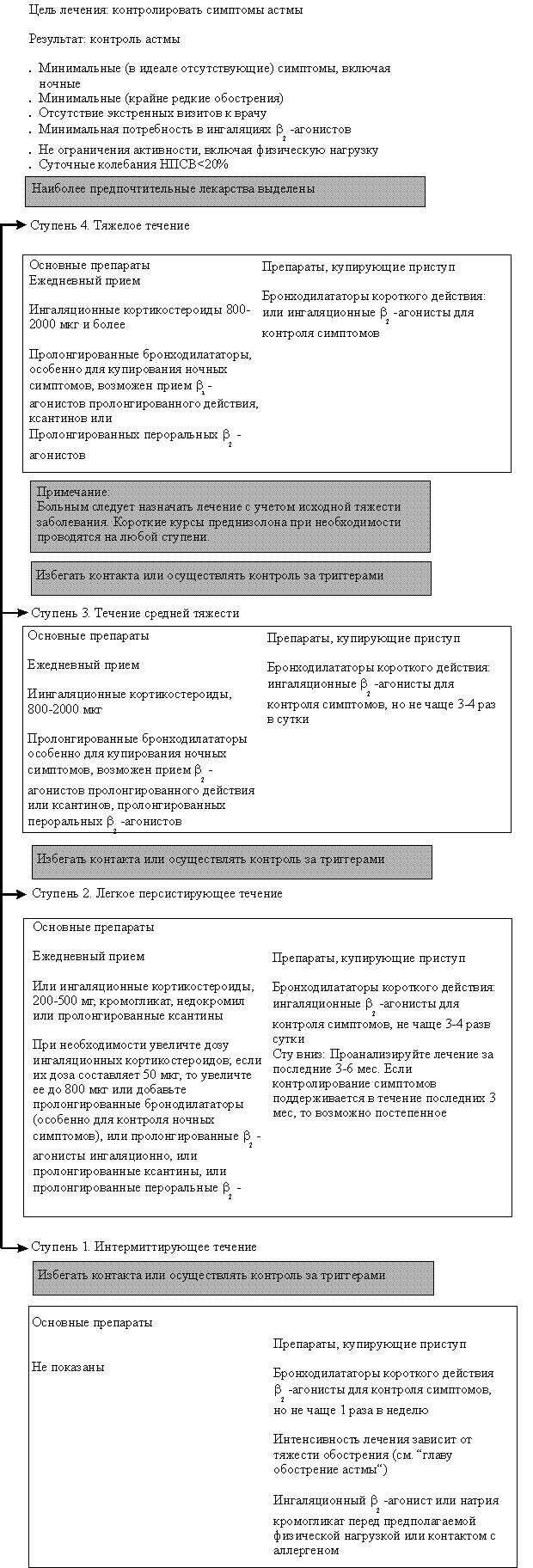
Подходы к лечению в зависимости от тяжести течения астмы показаны на рис. 2. Следует учитывать, что наименьшая тяжесть течения астмы представлена в 1-й ступени, а наибольшая — в 4-й ступени. Ступенчатый подход к лечению предусматривает подъем на более высокий уровень, если контроль над астмой не удается достичь или он потерян. Однако при этом необходимо учитывать, правильно ли больной принимает лекарства соответствующей ступени и нет ли контакта с аллергенами или другими провоцирующими факторами.
Контроль считается неудовлетворительным, если у больного наблюдаются:
|
Ступень 1. Больные с легким интермиттирующим течением астмы — это пациенты, у которых симптомы астмы появляются только при контакте с аллергенами (например, пыльца или шерсть животных) или обусловлены физической нагрузкой, а также дети, у которых свистящее дыхание возникает во время респираторно-вирусной инфекции нижних дыхательных путей.
Интермиттирующая астма — это не обычная форма болезни. Тяжесть обострений может значительно варьировать у различных больных в разное время. Такие обострения могут быть даже угрожающими для жизни, хотя это встречается крайне редко при интермиттирующем течении заболевания.
Длительная терапия противовоспалительными препаратами, как правило, не показана этим больным. Лечение включает профилактическй прием лекарств перед физической нагрузкой при необходимости (ингаляционные b 2-агонисты или кромогикат, или недокормил). Как альтернатива для ингаляционных b 2-агонистов короткого действия могут быть предложены антихолинергические препараты, пероральные b 2-агонисты короткого действия или тнофиллины короткого действия, хотя эти препараты начинают действие позднее и/или у них выше риск развития побочных проявлений.
Иногда более тяжелые и длительные обострения требуют назначения короткого курса пероральных кортикостероидов (см. рис. 2).
Ступень 2. Больные с легким персистирующим течением астмы нуждаются в ежедневном длительном профилактическом приеме лекарств для достижения и поддержания контроля над астмой. Первичная терапия — это прием противовоспалительных препаратов. Лечение можно начинать с ингаляционных кортикостероидов, кромогликата натрия или недокромила натрия. Предлагаемая доза кортикостероидов — 200 — 500 мкг беклометазона дипропионата или будесонида, или ингакорта, или другого эквивалента в день. Может быть предложена терапия теофиллинами пролонгированного действия. Однако необходимость контролировать концентрацию его в плазме (терапевтический разброс 5 — 15 мг/л) может сделать такое лечение не всегда возможным. Ингаляционные b 2-агонисты можно использовать для облегчения симптомов, но частота их приема не должна превышать 3 — 4 раз в сутки. Как альтернатива для ингаляционных b 2 -агонистов короткого действия могут быть предложены антихолинергические препараты, пероральные b 2 -агонисты короткого действия или теофиллины короткого действия, хотя эти препараты начинают действие позднее и/или у них выше риск развития побочных проявлений. Если больной принимает теофиллины пролонгированного действия, то прежде всего следует определить концентрацию теофиллина в плазме перед назначением теофиллинов короткого действия. При более тяжелых и длительных обострениях требуется назначение короткого курса пероральных кортикостероидов.
Если симптомы персистируют несмотря на начальную дозу ингаляционных кортикостероидов и врач уверен в том, что больной правильно использует препараты, дозу ингаляционных препаратов следует увеличить от 400 — 500 до 750 — 800 мкг в день (беклометазона дипропионат или эквивалент). Возможной альтернативой увеличению дозы ингаляционных гормонов, особенно для контроля ночных симптомов астмы (к дозе по крайней мере 500 мкг ингаляционных кортикостероидов), может быть назначение бронходилататоров пролонгированного действия на ночь.
Если контроля не удается достичь, что выражается более частыми симптомами, увеличением потребности в бронходилататорах или падением показателей ПСВ, то следует начать лечение по 3-й ступени.
Ступень 3. Больные со средней тяжестью течения астмы требуют ежедневного приема профилактических противовоспалительных препаратов для установления и поддержания контроля над астмой. Доза ингаляционных кортикостероидов должна быть на уровне 800 — 2000 мкг беклометазона дипротионата или его эквивалента. Рекомендуется использовать ингалятор со спейсером. Бронходилататоры длительного действия могут быть также назначены в добавление к ингаляционным кортикостероидам, особенно для контроля ночных симптомов. Можно применять теофиллины длительного действия, пероральные и ингаляционные b 2-агонисты длительного действия. Необходимо мониторировать концентрацию теофиллина длительного действия (обычный диапазон терапевтической концентрации 5 — 15 мкг на 1 мл). Купировать симптомы следует b 2-агонистами короткого действия или альтернативными препаратами, как описано во 2-й ступени. При более тяжелых обострениях можно проводить курс пероральных кортикостероидов.
Если контроля не удается достичь, что выражается более частыми симптомами, увеличением потребности в бронходилататорах, или падением показателей ПСВ, то следует начать лечение по 4-й ступени.
Рис. 1. Длительный контроль над астмой: диагностируйте и классифицируйте тяжесть течения
Рис.2. Длительный контроль над астмой: лечение с учетом ступенчатого подхода
Ступень 4. Больным с тяжелым течением бронхиальной астмы полностью контролировать астму не удается. Целью лечения становится достижение возможно лучших результатов: минимальное количество симптомов, минимальная потребность в b 2 -агонистах короткого действия, лучшие возможные показатели ПСВ, минимальный разброс ПСВ и минимальные побочные проявления от приема препаратов. Лечение обычно проводят с помощью большого количества контролирующих течение астмы препаратов.
Первичное лечение включает ингаляционные кортикостероиды в высоких дозах (от 800 до 2000 мкг в день беклометазона дипропионата или его эквивалента). В добавление к ингаляционным кортикостероидам рекомендуются пролонгированные бронходилататоры. Для достижения эффекта можно также 1 раз в день применять b 2 -агонисты короткого действия. Можно попробовать применить антихолинергический препарат (атровент), особенно больным, которые отмечают побочные явления при приеме b 2 -агонистов. При необходимости для облегчения симптомов можно использовать ингаляционные b 2 -агонисты короткого действия, но частота их приема не должна превышать 3 — 4 раз в сутки. Более тяжелое обострение может потребовать проведения курса пероральных кортикостероидов.
Длительное лечение пероральными кортикостероидами следует проводить в минимальных дозах или, если возможно, через день. Лечение высокими дозами ингаляционных кортикостероидов назначают через спейсер, что способствует более эффективному контролю и снижает некоторые побочные проявления.
Ступень вниз. Снижение поддерживающей терапии возможно, если астма остается под контролем не менее 3 мес. Это помогает снизить риск побочного действия и повышает восприимчивость больного к планируемому лечению. Уменьшать терапию следует ступенчато, понижая или отменяя последнюю дозу или дополнительные препараты. Необходимо наблюдать за симптомами, клиническими проявлениями и показателями ФВД.
Таким образом, хотя бронхиальная астма — заболевание неизлечимое, вполне уместно ожидать, что у большинства больных может и должен быть достигнут контроль за течением заболевания.
Важно также отметить, что подход к диагностике, классификации и лечению астмы с учетом тяжести ее течения позволяет создавать гибкие планы и специальные лечебные программы в зависимости от доступности противоастматических препаратов, системы регионального здравоохранения и особенностей конкретного больного.
1. Бронхиальная астма. Глобальная стратегия. Приложение к журналу Пульмонология. Москва. 1996;196.
2. Burney PGJ. Current questions in the epidemiology of asthma, in Holgate ST, et al (eds), Asthma: Physiology. Immunology, and Treatment. London, Academic Press, 1993;3-25.
3. Чучалин А.Г. Бронхиальная астма. М., 1985.
5. Wilson NM. Wheezy bronchitis revisited. Arch Dis Child 1989;64:1194-9.
6. Федосеев Г.Б., Емельянов А.В. Бронхиальная астма: трудные и нерешенные проблемы. Тер. арх. 1991;3:74-8.
7. Abramson MJ, et al. Evaluation of a new asthma questionnaire. J Asthma 1991;28:165-73.
8. Lebowitz MJ. The use of peak expiratory flow rate measurements in respiratory disease. Pediatr Pulmonol 1991;11:166-74.
9. Novak rm, et al. Comprison of peak expiratory flow and FEV1 admission criteria for acute bronchial asthma. Ann Emerg Med 1982;11:64-9.
10. Sporik R, Holgate ST, Codswell JJ. Natural history of asthma in childhood — a birth cohort study. Arch Dis Child 1991;66:1050-3.
11. Eggleston PA. Exercise — induced asthma, in Tinkelman DG, Npitz CK (eds), Childhood Asthma: Pathophysiology and Treatment, 2 nd. New York 6 Marcel Dekker, 1992;429-46.
12. Dow L, Coddon D, Holgate ST. Respiratory symptoms as predictors of airways in an elderly population. Respir Med 1992;146:402-7.
13. Cloutier MM, Loughlin GV. Chronic cough in children: a manifestation of airway hyperreactivity. Pediatrics 1981;67:6-12 Bousquet J, et al. Eosinophilic inflammation in asthm a. N Engl J Med 1990;323:1033-9.
14. Чучалин А.Г. Лечебные программы бронхиальной астмы. Тер. арх. 1987;3:111-6.
15. Bousquet J, et al. Eosinophilic inflammation in asthma. N Engl J Med 1990;323:1033-9.
16. British Thoracic Society, et al. Gui delines on the managment of asthma. Thorax 1993;48:1-24.
Источник