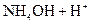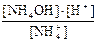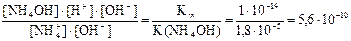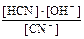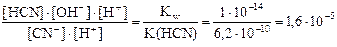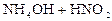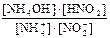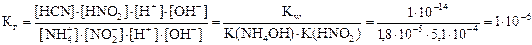Константа гидролиза
Основные понятия о константе гидролиза
В первом случае реакция чаще всего носит необратимый характер, т.е. вещество гидролизуется полностью. Из неорганических веществ гидролизу подвергаются соли: сначала происходит диссоциация на ионы, а после они взаимодействуют с молекулами воды с образованием слабого электролита. В данном случае процесс обратимый, т.е. устанавливается химическое равновесие и начинает «работать» закон действующих масс и можно записать выражение для константы равновесия, которая в данном случае будет называться константой гидролиза .
Допустим гидролизу подвергается соль состава АВ, образованная основанием АОН и кислотой НВ. Тогда уравнение гидролиза такой соли будет выглядеть следующим образом:
АВ↔ А + + В — (диссоциация соли);
А + + В — + НОН ↔АОН + НВ (ионное уравнение);
АВ+ НОН ↔АОН + НВ (молекулярное уравнение).
Выражение для константы равновесия этой реакции будет записываться:
Поскольку концентрация воды в разбавленных растворах величина постоянная Kg = K×[H2O], то выражение примет вид:
где Kg – константа гидролиза. Эта величина характеризует способность той или иной соли подвергаться гидролизу. Чем выше значение Kg, тем в большей степени протекает гидролиз.
Если соль гидролизуется по аниону, т.е. образована слабой кислотой и сильным основанием, то константа гидролиза связана с константой диссоциации кислоты:
Это означает, что, чем слабее кислота, тем сильнее её соли подвержены гидролизу.
Аналогично и для солей, гидролизующихся по катиону, т.е., образованных слабым основанием и сильной кислотой: чем слабее основание, тем в большей степени протекает гидролиз.
Примеры решения задач
| Задание | Составьте выражение для константы гидролиза карбоната натрия по первой ступени. Вычислите, если Kacid =4,8×10 -11 , а KH2O =10 -14 . |
| Решение | Карбонат натрия (Na2CO3) – соль, образованная слабой кислотой – угольной (H2CO3) и сильным основанием – гидроксидом натрия (NaOH). Гидролизуется по аниону. Среда щелочная. |
Запишем уравнение гидролиза по первой ступени:
Выражение для расчета константы равновесия будет записываться так:
А для константы гидролиза:
Рассчитаем константу гидролиза:
Kg =10 -14 / 4,8×10 -11 = 2×10 -4 .
| Задание | Запишите выражение для константы равновесия гидролиза нитрита натрия. |
| Решение | Нитрит натрия (NaNO2) – соль, образованная сильным основанием – гидроксидом натрия (NaOH) и слабой кислотой – азотистой (HNO2). Гидролизуется по аниону. Среда щелочная. |
Запишем уравнение гидролиза:
Выражение для расчета константы равновесия будет записываться так:
Источник
Гидролиз
Материалы портала onx.distant.ru
Теоретическое введение
Примеры обратимого гидролиза
Случаи необратимого гидролиза
Константа и степень гидролиза
Примеры решения задач
Задачи для самостоятельного решения
Теоретическое введение
Гидролиз – обменная реакция взаимодействия растворенного вещества (например, соли) с водой. Гидролиз происходит в тех случаях, когда ионы соли способны образовывать с Н + и ОН — ионами воды малодиссоциированные электролиты.
Примеры обратимого гидролиза
Соли, образованные сильным основанием и слабой кислотой, например , CH3COONa, Na2CO3, Na2S, KCN гидролизуются по аниону:
СН3СООNa + НОН ↔ СН3СООН + NaОН (рН > 7)
Гидролиз солей многоосновных кислот протекает ступенчато. 1 ступень:
CO3 2– + HOH ↔ HCO3 – + OH – ,
или в молекулярной форме:
или в молекулярной форме:
Продукты гидролиза по первой ступени подавляют вторую ступень гидролиза, в результате вторая ступень гидролиза протекает незначительно.
Соли, образованные слабым основанием и сильной кислотой, например , NH4Cl, FeCl3, Al2(SO4)3, гидролизуются по катиону:
или в молекулярной форме:
Соли, образованные многокислотными основаниями, гидролизуются ступенчато, образуя катионы основных солей. 1 ступень:
Fe 3+ + HOH ↔ FeOH 2+ + H + ;
FeCl3 + HOH ↔ FeOHCl2 + HCl
FeOH 2+ + HOH ↔ Fe(OH)2 + + H + ;
FeOHCl2 + HOH ↔ Fe(OH)2Cl+ HCl.
Fe(OH)2 + + HOH ↔ Fe(OH)3 + H + ;
Fe(OH)2Cl + HOH ↔ Fe(OH)3+ HCl.
Гидролиз по второй и, в особенности, по третьей ступени практически не протекает при комнатной температуре.
Соли, образованные слабым основанием и слабой кислотой, например , CH3COONH4, (NH4)2CO3, HCOONH4, гидролизуются и по катиону, и по аниону:
В этом случае реакция раствора зависит от соотношения констант диссоциации образующихся кислот и оснований. Поскольку в рассматриваемом примере константы диссоциации СH3COOH и NH3·H2О при 25 о С примерно равны (Кд(СH3COOH) = 1,75·10 –5 , Кд(NH3·H2О) = 1,76·10 –5 ), то раствор соли будет нейтральным.
При гидролизе HCOONH4 реакция раствора будет слабокислой, поскольку константа диссоциации муравьиной кислоты (Кд(HCOOН) = 1,77·10 –4 ) больше константы диссоциации уксусной кислоты.
Соли, образованные сильным основанием и сильной кислотой (например, NaNO3, KCl, Na2SO4), при растворении в воде гидролизу не подвергаются.
Случаи необратимого гидролиза
Гидролиз некоторых солей, образованных слабыми основаниями и слабыми кислотами, протекает необратимо. Необратимо гидролизуется, например , сульфид алюминия:
Следует отметить, что при смешении растворов солей гидролизующихся по аниону и катиону:
Mg 2+ + HOH ↔ MgOH + + H + ,
CO3 2– + HOH ↔ HCO3 – + OH –
Продукты гидролиза первой соли усиливают гидролиз второй соли и наоборот. В результате при смешении водных растворов сульфата магния и карбоната натрия образуется основной карбонат магния:
Основные карбонаты выпадают в осадок также при смешивании растворов карбонатов щелочных металлов и солей Be 2+ , Co 2+ , Ni 2+ , Zn 2+ , Pb 2+ , Cu 2+ и др.
При сливании растворов соды и солей Fe 2+ , Ca 2+ , Sr 2+ , Ba 2+ реакции протекают следующим образом:
(Ме – Fe, Ca, Sr, Ba)
При взаимодействии солей Аl 3+ , Сr 3+ и Fe 3+ в растворе с сульфидами, карбонатами и сульфитами в результате гидролиза в осадок выпадают не сульфиды, карбонаты и сульфиты этих катионов, а их гидроксиды:
Следует отметить, что катион Fe 3+ производит окисляющее действие на анион S 2- . В результате протекает реакция:
2Fe 3+ + S 2- = 2Fe 2+ + S о .
Например , хлорид железа (III) реагирует с сульфидом калия:
2FeCl3 + 3K2S = 2FeS + S + 6KCl
Некоторые соли в результате гидролиза в воде образуют малорастворимые оксосоединения:
SbCl3 + H2O → SbOCl↓ + 2HCl.
Необратимо гидролизуются в водных растворах галогенангидриды:
Константа и степень гидролиза
Константа Кг и α г степень гидролиза для растворов электролитов связаны между собой уравнением, по форме совпадающим с уравнением Оствальда:

Константа гидролиза Кг может быть рассчитана на основе значений ионного произведения воды Кw и константы диссоциации Кд образующихся в результате гидролиза слабой кислоты или слабого основания:

Примеры решения задач
Задача 1. Вычислите Кг, α г и рН 0,01 М раствора NH4Cl при температуре 298 К, если при указанной температуре Кд(NH3·H2O) = 1,76× 10 -5 .
Решение.

[Н + ] = 2,4·10 –4× 0,01 = 2,4× 10 –6 М.
рН = — lg 2,4× 10 –6 = 5,6.
Задача 2. Определите константу гидролиза, степень гидролиза и рН 0,02 М раствора НСООNa при 298 К, если при указанной температуре Кд(НСООН) = 1,77× 10 –4 .
Решение. Формиат натрия гидролизуется в соответствии с уравнением:
НСОО — + Н2О ↔ НСООН + ОН — .
Поскольку [НСООН] = [ОН – ] и [НСОО – ]·Сисх(НСООNa), то константу гидролиза можно записать следующим образом:


[Н + ] = 10 –14 ÷1,06× 10 –6 = 9,4·10 –9 М
рН = — lg 9,4× 10 –9 = 8
Задача 3. Определите рН 0,006М раствора NaNO2, если α г = 7·10 –3 %.
Решение.
[ОН – ] = 0,006× 7× 10 –5 = 4,2× 10 –7 М.
[Н + ] = 10 –14 :4,2× 10 –7 = 2,4× 10 –8 М.
рН = — lg 2,4× 10 –8 = 7,6.
Задача 5. Определите рН 0,1 М раствора Na3PO4 при 298 К, если константы диссоциации ортофосфорной кислоты при указанной температуре соответственно равны: Кд.1 = 7,11× 10 — 3 , Kд.2 = 6,34× 10 — 8 , Kд.3 = 4,40× 10 — 13 .
Решение. Na3PO4 диссоциирует в растворе и подвергается ступенчатому гидролизу:
Следует обратить внимание на выбор “нужной” величины Кд.
Kдисс.2 = 6,34·10 — 8
Так как Кг,1 > > Кг,2, то можно считать, что соль подвергается гидролизу только по первой ступени.

поскольку [HPO4 2- ] = [OH — ].
рОН = –lg 4,76× 10 — 2 = 1,32 и рН = 14 – 1,32 = 12,68.
Задачи для самостоятельного решения
1. Гидролиз соли Na2SO3 усилится при добавлении в раствор веществ:
| а) Н2O | б) Na2CO3 | в) NaOH |
| г) H2SO4 | д) Na2S | е) Na2SO4 |
2. Напишите уравнение реакции NiCl2 + Na2CO3 + H2O → .
Источник
Константа и степень гидролиза
Количественной характеристикой обратимого гидролиза солей являются константа гидролиза и степень гидролиза. Константа гидролиза – это константа равновесия обратимой реакции гидролиза; она обозначается Кг (г – «гидролиз») или Kh (h – «hidrolys»). Степень гидролиза αг (или h) представляет собой отношение числа молекул, подвергшихся гидролизу, к общему числу молекул. Константа и степень гидролиза связаны между собой в соответствии с законом разбавления Оствальда.
Если соль гидролизуется только по катиону или только по аниону, то его косвенным количественным показателем является также водородный показатель: чем полнее идёт гидролиз, тем в большей степени pH отличается от числа 7 – водородного показателя нейтральной среды.
Пример 24.Вычислите константу гидролиза хлорида аммония, степень гидролиза в 0,1 М растворе и pH этого раствора. По результатам вычислений сделайте вывод.
Решение. 1) Записываем уравнение гидролиза в молекулярном и ионном виде:
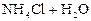
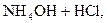
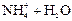
и выражение константы гидролиза:
Кг =
2) Умножая числитель и знаменатель правой части выражения на концентрацию гидроксид-ионов, получаем формулу для расчёта константы гидролиза; вычисляем её по справочным данным:
Кг =
3) По закону разбавления Оствальда вычисляем степень гидролиза:
αг 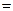
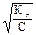
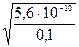
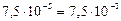
4) Рассчитываем концентрацию ионов водорода:
[H + ] = αг∙С = 7,5∙10 –5 0,1 = 7,5∙10 –6
5) Вычисляем водородный показатель раствора:
pH = –lg[H + ] = –lg(7,5∙10 –6 ) = 5,1
Из полученных результатов следует, что гидролиз хлорида аммония протекает в незначительной степени, но, тем не менее, среда раствора кислая.
Пример 25. Вычислите константу гидролиза цианида калия, степень гидролиза в 0,1 М растворе и рН этого раствора. По результатам вычислений сделайте вывод.
Решение. Последовательность решения такая же, как и в предыдущем примере, только во втором действии правую часть выражения для константы гидролиза умножаем и делим на концентрацию катионов водорода.
1) 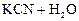
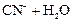
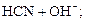
2) Кг =
3) αг 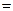
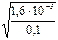
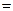
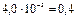
4) [ОН – ] = αг∙С = 4,0∙10 –3 0,1 = 4,0∙10 –4
5) pОH = –lg[ОH – ] = –lg(4,0∙10 –4 ) = 3,4
6) pH = 14 – pOH = 14 – 3,4 = 11,6
Из полученных результатов следует, что гидролиз цианида калия протекает в незначительной степени, но полнее, чем хлорида аммония, поскольку HCN является менее сильным электролитом, чем NH4OH; среда раствора щелочная.
Пример 26. Вычислите константу гидролиза нитрита аммония степень гидролиза в децимолярном растворе. Сделайте вывод, определите среду раствора.
Решение. 1) Записываем уравнение и выражение константы гидролиза:
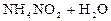
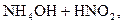
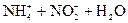
Кг =
2) Умножаем числитель и знаменатель правой части выражения константы гидролиза на концентрацию катионов Н + и анионов ОН — , получаем формулу для расчёта константы гидролиза по справочным данным:
3) Вычисляем степень гидролиза:
αг 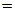
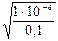
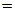
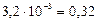
Из полученных результатов следует, что гидролиз протекает обратимо; среда раствора кислая, так как из двух образующихся слабых электролитов (NH4OH и HNO2) азотистая кислота имеет большее значение константы диссоциации.
Нам важно ваше мнение! Был ли полезен опубликованный материал? Да | Нет
Источник