- Гидролиз
- Гидролиз нитрата серебра (I)
- Общие сведения о гидролизе нитрата серебра (I)
- Гидролиз нитрата серебра (I)
- Примеры решения задач
- Agno3 гидролиз по ступенями
- Гидролиз
- Теоретическое введение
- Примеры обратимого гидролиза
- Случаи необратимого гидролиза
- Константа и степень гидролиза
- Примеры решения задач
- Задачи для самостоятельного решения
Гидролиз
Гидролиз (греч. hydor — вода и lysis — разрушение) — процесс расщепления молекул сложных химических веществ за счет реакции с молекулами воды.
В химии, как и в жизни, разрушается чаще всего нестойкое и слабое (стойкое и сильное выдерживает удар). Запомните, что гидролиз (вода) разрушает «слабое» — это правило вам очень пригодится.
Любая соль состоит из остатка основания и кислоты. Абсолютно любая:
- NaCl — производное основания NaOH и кислоты HCl
- KNO3 — производное основания KOH и кислоты HNO3
- CuSO4 — производное основания Cu(OH)2 и кислоты H2SO4
- Al3PO4 — производное основания Al(OH)3 и кислоты H3PO4
- Ca(NO2)2 — производное основания Ca(OH)2 и кислоты HNO2
Чтобы успешно решать задания по теме гидролиза и писать реакции, вам следует запомнить, какие основания и кислоты являются слабыми, а какие — сильными.
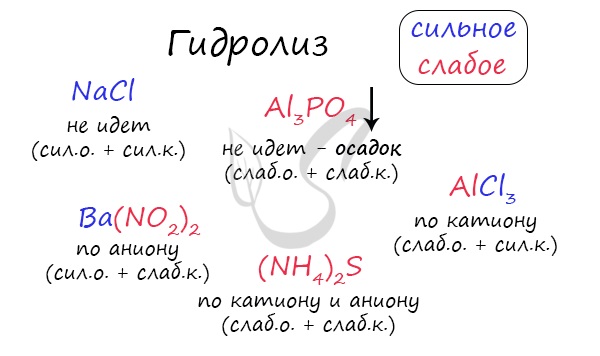
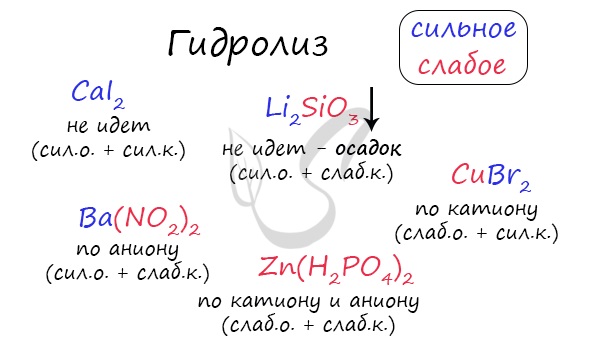
При изучении гидролиза я рекомендую ученикам сохранить на гаджет схему, которую вы видите ниже. Для того, чтобы приобрести нужный опыт — она незаменима. Пользуйтесь ей как можно чаще, подглядывайте в нее и она незаметно окажется в вашем интеллектуальном составляющем 😉
По катиону, по аниону или нет гидролиза?
Итак, если в состав соли входит остаток сильного основания и остаток сильной кислоты — гидролиза не происходит. Примеры: NaCl, KBr, CaSO4. Также гидролиза не происходит, если соль нерастворима (вне зависимости от того, чем она образована): AlPO4, FeSO3, CaSO3.
Если в состав соли входит остаток слабого основания и остаток сильной кислоты, то гидролиз идет по катиону. Помните, что гидролиз разрушает слабое, в данном случае — катион. Примеры: AlCl3, MgBr2, Cr2SO4, NH4NO3.
Катион NH4 + и его основание NH4OH , несмотря на растворимость, является слабым, поэтому гидролиз будет идти по катиону в соли NH4Cl. Замечу также, что Ca(OH)2 считается растворимым основанием, поэтому гидролиза соли CaCl2 не происходит.
Если в состав соли входит остаток сильного основания и остаток слабой кислоты, то гидролиз идет по аниону. Примеры: K3PO4, NaNO2, Ca(OCl)2, Ba(CH3COO)2, Li2SiO3.
Если соль образована остатком слабого основания и слабой кислоты, то гидролиз идет и по катиону, и по аниону. Примеры: Mg(NO2)2, Al2S3, Cr2(SO3)3, CH3COONH4.
Среда раствора
Среда раствора может быть нейтральной, кислой или щелочной. Определяется типом гидролиза. Некоторые задания могут быть построены так, что, увидев соль, вы должны будете определить ее тип раствора.
Обрадую вас: если вы усвоили тему гидролиза, сделать это проще простого. В случае, когда гидролиз не идет или идет и по катиону, и по аниону среда раствора — нейтральная.
Если гидролиз идет по катиону (разрушается остаток основания) среда — кислая, если гидролиз идет по аниону (разрушается остаток кислоты), то среда раствора будет щелочная. Изучите примеры.
Однако замечу, что в дигидрофосфатах, гидросульфитах и гидросульфатах среда всегда кислая из-за особенностей диссоциации. Примеры: NH4H2PO4, LiHSO4. В гидрофосфатах среда щелочная из-за того, что константа диссоциации по третьей ступени меньше, чем константа гидролиза. Примеры: K2HPO4, Na2HPO4.
Попробуйте определить среду раствора для соединений из самостоятельного задания, которое вы только что решили. Ниже будет располагаться решение.
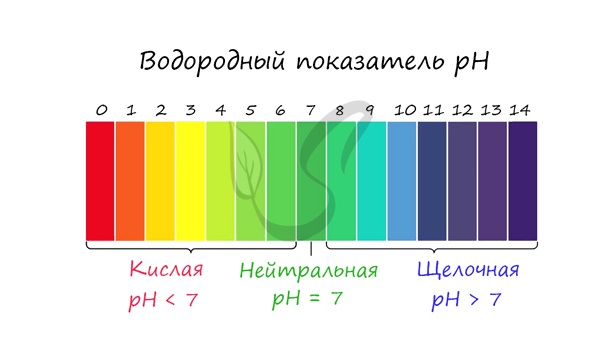
С целью запутать в заданиях часто бывают даны синонимы. Так «среду раствора» могут заменить водородным показателем pH.
Запомните, что кислая среда характеризуется pH 7.
Например, в соли CaCl2 среда раствора будет нейтральной (pH=7), а в растворе AlCl3 — кислой (pH
Источник
Гидролиз нитрата серебра (I)
Общие сведения о гидролизе нитрата серебра (I)
Представляет собой бесцветные кристаллы ромбической формы. Молярная масса – 170 г/моль.
Рис. 1. Нитрат серебра (I). Внешний вид.
Гидролиз нитрата серебра (I)
Гидролизуется по катиону. Характер среды – кислый. Уравнение гидролиза имеет следующий вид:
AgNO3 ↔ Ag + + NO3 — (диссоциация соли);
Ag + +HOH ↔ AgOH+ H + (гидролиз по катиону);
Ag + + NO3 — + HOH ↔ AgOH + NO3 — + H + (ионное уравнение);
AgNO3+ H2O↔ AgOH + HNO3 (молекулярное уравнение).
Примеры решения задач
| Задание | Рассчитайте массовые доли каждого из элементов, входящих в состав нитрата серебра (I). |
| Решение | Массовая доля элемента рассчитывается следующим образом: |
т.е. отношение относительной атомной массы с учетом количества атомов, входящих в состав вещества, к молекулярной массе этого вещества, выраженное в процентах. Молекулярная масса нитрата серебра (I) равна 170.
Рассчитаем массовые доли элементов:
ω(Ag) = 1×108/170 ×100% =63,53%.
ω(N) = 1×14/170 ×100% =8,23%.
ω(O) = 3×16/170 ×100% =28,24%.
Чтоб проверить правильность расчета, путем складывания полученных массовых долей мы должны получить 100%:
ω(Ag) +ω(N) +ω(O) = 63,53 +8,23+28,24 = 100%.
| Задание | Установите соответствие между формулой соли и ионным уравнением её гидролиза. Ответ обоснуйте. | ||||||||
| Ответ | Соль дигидрофосфат натрия (NaH2PO4) гидролизуется по аниону H2PO4 — , поскольку образована слабой кислотой – ортофосфорной и сильным основанием – гидроксидом натрия (1). Соль перхлорат калия (KClO4) гидролизу не подвергается, поскольку образована сильным основанием – гидроксидом калия и сильной кислотой – хлорной (4). Соль сульфат бериллия (BeSO4) гидролизуется по катиону Be 2+ , поскольку образована слабым основанием – гидроксидом бериллия и сильной кислотой – серной (2). Соль карбонат кальция (CaCO3) гидролизуется по аниону CO3 2- , поскольку образована слабой кислотой – угольной и сильным основанием – гидроксидом кальция (3). Источник Agno3 гидролиз по ступенямиУстановите соответствие между формулой соли и типом гидролиза её водного раствора: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
Запишите в ответ цифры, расположив их в порядке, соответствующем буквам: Eсли растворимая соль образована сильной кислотой и слабым основанием, то она гидролизуется по катиону (части слабого основания). Например, В результате раствор имеет кислую среду (избыток ионов водорода). Eсли растворимая соль образована слабой кислотой и сильным основанием, то она гидролизуется по аниону (части слабой кислоты). Например, В результате раствор имеет щелочную среду (избыток гидроксид-ионов). Соль, образованная сильной кислотой и сильным основанием, не гидролизуется, среда нейтральная. Растворимая соль, образованная слабой кислотой и слабым основанием, гидролизуется и по катиону, и по аниону. Нерастворимые соли гидролизу не подвергаются. А) Карбонат кальция — нерастворимая соль — реакция среды — гидролиза нет (3). Б) Нитрат серебра — не гидролизуется (3). В) Хлорид аммония — образован сильной кислотой и слабым основанием — гидролиз по катиону (1). Г) Хлорид натрия — образован сильной кислотой и сильным основанием — гидролиза нет (3). Примечание: нитрат серебра не подвергается гидролизу, можно считать это «исключением из правил», этот факт нужно запомнить. Источник ГидролизМатериалы портала onx.distant.ru Теоретическое введение Примеры обратимого гидролиза Случаи необратимого гидролиза Константа и степень гидролиза Примеры решения задач Задачи для самостоятельного решения Теоретическое введениеГидролиз – обменная реакция взаимодействия растворенного вещества (например, соли) с водой. Гидролиз происходит в тех случаях, когда ионы соли способны образовывать с Н + и ОН — ионами воды малодиссоциированные электролиты. Примеры обратимого гидролизаСоли, образованные сильным основанием и слабой кислотой, например , CH3COONa, Na2CO3, Na2S, KCN гидролизуются по аниону: СН3СООNa + НОН ↔ СН3СООН + NaОН (рН > 7) Гидролиз солей многоосновных кислот протекает ступенчато. 1 ступень: CO3 2– + HOH ↔ HCO3 – + OH – , или в молекулярной форме: или в молекулярной форме: Продукты гидролиза по первой ступени подавляют вторую ступень гидролиза, в результате вторая ступень гидролиза протекает незначительно. Соли, образованные слабым основанием и сильной кислотой, например , NH4Cl, FeCl3, Al2(SO4)3, гидролизуются по катиону: или в молекулярной форме: Соли, образованные многокислотными основаниями, гидролизуются ступенчато, образуя катионы основных солей. 1 ступень: Fe 3+ + HOH ↔ FeOH 2+ + H + ; FeCl3 + HOH ↔ FeOHCl2 + HCl FeOH 2+ + HOH ↔ Fe(OH)2 + + H + ; FeOHCl2 + HOH ↔ Fe(OH)2Cl+ HCl. Fe(OH)2 + + HOH ↔ Fe(OH)3 + H + ; Fe(OH)2Cl + HOH ↔ Fe(OH)3+ HCl. Гидролиз по второй и, в особенности, по третьей ступени практически не протекает при комнатной температуре. Соли, образованные слабым основанием и слабой кислотой, например , CH3COONH4, (NH4)2CO3, HCOONH4, гидролизуются и по катиону, и по аниону: В этом случае реакция раствора зависит от соотношения констант диссоциации образующихся кислот и оснований. Поскольку в рассматриваемом примере константы диссоциации СH3COOH и NH3·H2О при 25 о С примерно равны (Кд(СH3COOH) = 1,75·10 –5 , Кд(NH3·H2О) = 1,76·10 –5 ), то раствор соли будет нейтральным. При гидролизе HCOONH4 реакция раствора будет слабокислой, поскольку константа диссоциации муравьиной кислоты (Кд(HCOOН) = 1,77·10 –4 ) больше константы диссоциации уксусной кислоты. Соли, образованные сильным основанием и сильной кислотой (например, NaNO3, KCl, Na2SO4), при растворении в воде гидролизу не подвергаются. Случаи необратимого гидролизаГидролиз некоторых солей, образованных слабыми основаниями и слабыми кислотами, протекает необратимо. Необратимо гидролизуется, например , сульфид алюминия: Следует отметить, что при смешении растворов солей гидролизующихся по аниону и катиону: Mg 2+ + HOH ↔ MgOH + + H + , CO3 2– + HOH ↔ HCO3 – + OH – Продукты гидролиза первой соли усиливают гидролиз второй соли и наоборот. В результате при смешении водных растворов сульфата магния и карбоната натрия образуется основной карбонат магния: Основные карбонаты выпадают в осадок также при смешивании растворов карбонатов щелочных металлов и солей Be 2+ , Co 2+ , Ni 2+ , Zn 2+ , Pb 2+ , Cu 2+ и др. При сливании растворов соды и солей Fe 2+ , Ca 2+ , Sr 2+ , Ba 2+ реакции протекают следующим образом: (Ме – Fe, Ca, Sr, Ba) При взаимодействии солей Аl 3+ , Сr 3+ и Fe 3+ в растворе с сульфидами, карбонатами и сульфитами в результате гидролиза в осадок выпадают не сульфиды, карбонаты и сульфиты этих катионов, а их гидроксиды: Следует отметить, что катион Fe 3+ производит окисляющее действие на анион S 2- . В результате протекает реакция: 2Fe 3+ + S 2- = 2Fe 2+ + S о . Например , хлорид железа (III) реагирует с сульфидом калия: 2FeCl3 + 3K2S = 2FeS + S + 6KCl Некоторые соли в результате гидролиза в воде образуют малорастворимые оксосоединения: SbCl3 + H2O → SbOCl↓ + 2HCl. Необратимо гидролизуются в водных растворах галогенангидриды: Константа и степень гидролизаКонстанта Кг и α г степень гидролиза для растворов электролитов связаны между собой уравнением, по форме совпадающим с уравнением Оствальда: Константа гидролиза Кг может быть рассчитана на основе значений ионного произведения воды Кw и константы диссоциации Кд образующихся в результате гидролиза слабой кислоты или слабого основания: Примеры решения задачЗадача 1. Вычислите Кг, α г и рН 0,01 М раствора NH4Cl при температуре 298 К, если при указанной температуре Кд(NH3·H2O) = 1,76× 10 -5 . Решение.
[Н + ] = 2,4·10 –4× 0,01 = 2,4× 10 –6 М. рН = — lg 2,4× 10 –6 = 5,6. Задача 2. Определите константу гидролиза, степень гидролиза и рН 0,02 М раствора НСООNa при 298 К, если при указанной температуре Кд(НСООН) = 1,77× 10 –4 . Решение. Формиат натрия гидролизуется в соответствии с уравнением: НСОО — + Н2О ↔ НСООН + ОН — . Поскольку [НСООН] = [ОН – ] и [НСОО – ]·Сисх(НСООNa), то константу гидролиза можно записать следующим образом:
[Н + ] = 10 –14 ÷1,06× 10 –6 = 9,4·10 –9 М рН = — lg 9,4× 10 –9 = 8 Задача 3. Определите рН 0,006М раствора NaNO2, если α г = 7·10 –3 %. Решение. [ОН – ] = 0,006× 7× 10 –5 = 4,2× 10 –7 М. [Н + ] = 10 –14 :4,2× 10 –7 = 2,4× 10 –8 М. рН = — lg 2,4× 10 –8 = 7,6. Задача 5. Определите рН 0,1 М раствора Na3PO4 при 298 К, если константы диссоциации ортофосфорной кислоты при указанной температуре соответственно равны: Кд.1 = 7,11× 10 — 3 , Kд.2 = 6,34× 10 — 8 , Kд.3 = 4,40× 10 — 13 . Решение. Na3PO4 диссоциирует в растворе и подвергается ступенчатому гидролизу: Следует обратить внимание на выбор “нужной” величины Кд. Kдисс.2 = 6,34·10 — 8 Так как Кг,1 > > Кг,2, то можно считать, что соль подвергается гидролизу только по первой ступени.
поскольку [HPO4 2- ] = [OH — ]. рОН = –lg 4,76× 10 — 2 = 1,32 и рН = 14 – 1,32 = 12,68. Задачи для самостоятельного решения1. Гидролиз соли Na2SO3 усилится при добавлении в раствор веществ:
2. Напишите уравнение реакции NiCl2 + Na2CO3 + H2O → . Источник |





 (1)
(1) (2)
(2) .
.

 .
.




 ,
,